主な薬効は、抗真菌作用、 白癬に対する作用 です。
商品名
禁忌
警告
-
重篤な肝障害(肝不全、肝炎、胆汁うっ滞、黄疸等)及び汎血球減少、無顆粒球症、血小板減少があらわれることがあり、死亡に至った例も報告されている。本剤を使用する場合には、投与前に肝機能検査及び血液検査を行い、本剤の投与中は随伴症状に注意し、定期的に肝機能検査及び血液検査を行うなど観察を十分に行うこと。(【禁忌】、「重要な基本的注意」、「副作用」の項参照)
本剤の投与開始にあたっては、添付文書を熟読すること。
禁忌(次の患者には投与しないこと)
|
効果・効能
一般的名称: ;
効能又は効果
関連する疾病:
カンジダ性指間びらん, カンジダ性間擦疹, 乳児寄生菌性紅斑, 指間カンジダ症, 皮膚カンジダ症, 紅斑性間擦疹, 皮膚真菌症, カンジダ症, 皮膚びらん, 体部白癬, 股部白癬, 真菌症, 足白癬, 間擦疹, 紅斑症, 白癬, 癜風
用法及び用量
- 1日1回患部に塗布する。
一般的名称: ;
効能又は効果
関連する疾病:
カンジダ性指間びらん, カンジダ性間擦疹, 乳児寄生菌性紅斑, 指間カンジダ症, 皮膚カンジダ症, 紅斑性間擦疹, 皮膚真菌症, カンジダ症, 皮膚びらん, 体部白癬, 股部白癬, 真菌症, 足白癬, 間擦疹, 紅斑症, 白癬, 癜風
用法及び用量
- 1日1回患部に塗布する。
一般的名称: ;
効能又は効果
関連する疾病:
カンジダ性指間びらん, カンジダ性間擦疹, 乳児寄生菌性紅斑, 指間カンジダ症, 皮膚カンジダ症, 紅斑性間擦疹, 皮膚真菌症, カンジダ症, 皮膚びらん, 体部白癬, 股部白癬, 真菌症, 足白癬, 間擦疹, 紅斑症, 白癬, 癜風
用法及び用量
- 1日1回患部に噴霧する。
一般的名称: ;
効能又は効果
- 皮膚糸状菌(トリコフィトン属、ミクロスポルム属、エピデルモフィトン属)、カンジダ属、スポロトリックス属、ホンセカエア属による下記感染症。
但し、外用抗真菌剤では治療困難な患者に限る。
関連する疾病:
肺スポロトリコーシス, 脳クロモミコーシス, スポロトリクム症, クロモミコーシス, 深在性皮膚真菌症, 皮膚カンジダ症, 白癬菌性肉芽腫, 角質増殖型白癬, 皮膚糸状菌症, 深在性真菌症, ケルスス禿瘡, 爪カンジダ症, 皮膚真菌症, カンジダ症, 皮膚感染症, 深在性白癬, 皮膚肉芽腫, 白癬性毛瘡, 糸状菌症, 頭部白癬, 足爪白癬, 趾間白癬, 趾部白癬, 真菌症, 爪白癬, 手白癬, 足白癬, 白癬, 禿瘡, 毛瘡
効能又は効果に関連する使用上の注意
- 本剤の投与は、罹患部位、重症度及び感染の範囲より本剤の内服が適切と判断される患者にのみ使用し、外用抗真菌剤で治療可能な患者には使用しないこと。
関連する疾病:
用法及び用量
- 通常、成人にはテルビナフィンとして125mgを1日1回食後に経口投与する。なお、年齢、症状により適宜増減する。
用法及び用量に関連する使用上の注意
- 本剤の投与中は随伴症状に注意し、定期的に肝機能検査及び血液検査(血球数算定、白血球分画等)を行うなど観察を十分に行うこと。(「副作用」の項参照)
臨床成績
一般的名称: ;
臨床成績
- 比較試験を含む645例について行われた1日1回塗布による本剤の臨床試験成績は次のとおりである。
- 疾患・病型/白癬:足白癬
- 有効率:74.3%(142/191)
- 疾患・病型/白癬:体部白癬
- 有効率:85.6%(83/97)
- 疾患・病型/白癬:股部白癬
- 有効率:91.5%(75/82)
- 疾患・病型/皮膚カンジダ症:指間びらん症
- 有効率:85.2%(23/27)
- 疾患・病型/皮膚カンジダ症:間擦疹
- 有効率:91.3%(84/92)
- 疾患・病型/癜風
- 有効率:87.0%(67/77)
-
2.
その他 - 健康成人の無傷背部皮膚表面にテルビナフィン塩酸塩1%クリーム及び基剤を用いたパッチテスト並びに光パッチテストの結果では、皮膚刺激性は認められていない。
1.
臨床試験成績
一般的名称: ;
臨床成績
- 1日1回塗布による本剤の臨床試験成績は次のとおりである。
- 疾患・病型/白癬:足白癬
- 有効率:69.7%(46/66)
- 疾患・病型/白癬:体部白癬
- 有効率:75.0%(9/12)
- 疾患・病型/白癬:股部白癬
- 有効率:100.0%(7/7)
- 疾患・病型/皮膚カンジダ症:指間びらん症
- 有効率:100.0%(3/3)
- 疾患・病型/皮膚カンジダ症:間擦疹
- 有効率:81.8%(9/11)
- 疾患・病型/癜風
- 有効率:71.4%(5/7)
-
2.
その他 - 健康成人の無傷背部皮膚表面にテルビナフィン塩酸塩1%液及び基剤を用いたパッチテスト並びに光パッチテストの結果では、皮膚感作性は認められていない。
1.
臨床試験成績
一般的名称: ;
臨床成績
- 1日1回塗布による臨床試験成績は次のとおりである(ラミシール外用液1%)。
- 疾患・病型:白癬(足白癬)
- 有効率:69.7%(46/66)
- 疾患・病型:白癬(体部白癬)
- 有効率:75.0%(9/12)
- 疾患・病型:白癬(股部白癬)
- 有効率:100.0%(7/7)
- 疾患・病型:皮膚カンジダ症(指間びらん症)
- 有効率:100.0%(3/3)
- 疾患・病型:皮膚カンジダ症(間擦疹)
- 有効率:81.8%(9/11)
- 疾患・病型:癜風
- 有効率:71.4%(5/7)
-
2.
その他 - 健康成人の無傷背部皮膚表面にテルビナフィン塩酸塩1%液及び基剤を用いたパッチテスト並びに光パッチテストの結果では、皮膚感作性は認められていない。
1.
臨床試験成績
一般的名称: ;
臨床成績
- 比較試験を含む有効性解析対象554例について1日1回投与による本剤の臨床試験成績は次のとおりである。
臨床試験成績
副作用
一般的名称: ;
副作用
- 総症例8,910例中何らかの副作用が報告されたのは、161例(1.81%)であった。主な副作用は接触皮膚炎82件(0.92%)、そう痒感36件(0.40%)、発赤35件(0.39%)、刺激感31件(0.35%)等であった。(ラミシールクリーム1%・外用液1%の承認時まで及び再審査終了時までの集計)
-
1.
過敏症 - (頻度不明)
- 発疹、蕁麻疹、血管浮腫
-
2.
過敏症 - (0.1%〜5%未満)
- そう痒症、紅斑
-
3.
適用部位 - (頻度不明)
- 湿疹、皮膚乾燥、疼痛、色素沈着、皮膚灼熱感
-
4.
適用部位 - (0.1%〜5%未満)
- 接触皮膚炎、発赤、刺激感
-
5.
適用部位 - (0.1%未満)
- 鱗屑、落屑、皮膚亀裂
- 以上のような副作用があらわれた場合には、使用を中止するなど、適切な処置を行うこと。
- 妊婦、産婦、授乳婦等への使用
- 妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。〔妊娠中の使用に関する安全性は確立していない。〕
- 小児等への使用
- 低出生体重児、新生児に対する安全性は確立していない(使用経験が少ない)。
一般的名称: ;
副作用
- 総症例8,910例中何らかの副作用が報告されたのは、161例(1.81%)であった。主な副作用は接触皮膚炎82件(0.92%)、そう痒感36件(0.40%)、発赤35件(0.39%)、刺激感31件(0.35%)等であった。(ラミシールクリーム1%・外用液1%の承認時まで及び再審査終了時までの集計)
-
1.
過敏症 - (頻度不明)
- 発疹、蕁麻疹、血管浮腫
-
2.
過敏症 - (0.1%〜5%未満)
- そう痒症、紅斑
-
3.
適用部位 - (頻度不明)
- 湿疹、皮膚乾燥、疼痛、色素沈着、皮膚灼熱感
-
4.
適用部位 - (0.1%〜5%未満)
- 接触皮膚炎、発赤、刺激感
-
5.
適用部位 - (0.1%未満)
- 鱗屑、落屑、皮膚亀裂
- 以上のような副作用があらわれた場合には、使用を中止するなど、適切な処置を行うこと。
- 妊婦、産婦、授乳婦等への使用
- 妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。〔妊娠中の使用に関する安全性は確立していない。〕
- 小児等への使用
- 低出生体重児、新生児に対する安全性は確立していない(使用経験がない)。
一般的名称: ;
副作用
- 総症例8,910例中何らかの副作用が報告されたのは、161例(1.81%)であった。主な副作用は接触皮膚炎82件(0.92%)、そう痒感36件(0.40%)、発赤35件(0.39%)、刺激感31件(0.35%)等であった。(ラミシールクリーム1%・外用液1%の承認時まで及び再審査終了時までの集計)
-
1.
過敏症 - (頻度不明)
- 発疹、蕁麻疹、血管浮腫
-
2.
過敏症 - (0.1%〜5%未満)
- そう痒症、紅斑
-
3.
適用部位 - (頻度不明)
- 湿疹、皮膚乾燥、疼痛、色素沈着、皮膚灼熱感
-
4.
適用部位 - (0.1%〜5%未満)
- 接触皮膚炎、発赤、刺激感
-
5.
適用部位 - (0.1%未満)
- 鱗屑、落屑、皮膚亀裂
- 以上のような副作用があらわれた場合には、使用を中止するなど、適切な処置を行うこと。
一般的名称: ;
副作用
副作用等発現状況の概要
-
承認時までの調査767例中、何らかの副作用(自他覚症状又は臨床検査値異常)が報告されたのは81例(10.56%)であった。主な自他覚症状は、胃部不快感29件(3.78%)、下痢15件(1.96%)、悪心14件(1.83%)、腹痛13件(1.69%)、胃部膨満感10件(1.30%)、めまい8件(1.04%)、発疹7件(0.91%)、頭痛6件(0.78%)、食欲不振4件(0.52%)等であった。また、主な臨床検査値異常は、AST(GOT)上昇13件(1.69%)、ALT(GPT)上昇12件(1.56%)、γ-GTP上昇8件(1.04%)、LDH上昇5件(0.65%)等であった。
市販後の使用成績調査6,929例中、何らかの副作用(自他覚症状又は臨床検査値異常)が報告されたのは825例(11.91%)であった。主な自他覚症状は、胃部不快感114件(1.65%)、肝障害・肝機能異常等の肝胆道系障害106件(1.53%)、腹痛53件(0.76%)、悪心37件(0.53%)等であった。また、主な臨床検査値異常は、白血球減少90件(1.30%)、γ-GTP上昇72件(1.04%)、貧血62件(0.89%)、ALT(GPT)上昇51件(0.74%)、LDH上昇42件(0.61%)等であった。
(承認時まで及び再審査終了時までの集計)
重大な副作用
- 1. 重篤な肝障害(肝不全、肝炎、胆汁うっ滞、黄疸等)(0.01%)
- 発疹、皮膚そう痒感、発熱、悪心・嘔吐、食欲不振、けん怠感等の随伴症状に注意するとともに、投与開始後2ヵ月間は月1回の肝機能検査を行うこと。また、その後も定期的に肝機能検査を行うなど観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。
- 2. 汎血球減少、無顆粒球症、血小板減少(いずれも頻度不明)
- 咽頭炎、発熱、リンパ節腫脹、紫斑、皮下出血等の随伴症状に注意し、定期的に血液検査(血球数算定、白血球分画等)を行うなど観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。
- 3. 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、急性全身性発疹性膿疱症、紅皮症(剥脱性皮膚炎)(いずれも頻度不明)
- 中毒性表皮壊死融解症、皮膚粘膜眼症候群、急性全身性発疹性膿疱症、紅皮症(剥脱性皮膚炎)があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。
- 4. 横紋筋融解症(頻度不明)
- 横紋筋融解症があらわれることがあるので、観察を十分に行い、筋肉痛、脱力感、CK(CPK)上昇、血中及び尿中ミオグロビン上昇が認められた場合には投与を中止し、適切な処置を行うこと。
- 5. ショック、アナフィラキシー(いずれも頻度不明)
- ショック、アナフィラキシーがあらわれることがあるので、観察を十分に行い、呼吸困難、全身潮紅、血管浮腫、蕁麻疹等の症状が認められた場合には投与を中止し、適切な処置を行うこと。
- 6. 薬剤性過敏症候群(頻度不明)
- 初期症状として発疹、発熱がみられ、更に肝機能障害、リンパ節腫脹、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがあるので、観察を十分に行い、このような症状があらわれた場合には投与を中止し、適切な処置を行うこと。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること。
- 7. 亜急性皮膚エリテマトーデス(頻度不明)
- 亜急性皮膚エリテマトーデスがあらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。
その他の副作用
- 1. 過敏症
- (頻度不明)
- 乾癬様発疹、血清病様反応
- 2. 過敏症
- (0.1%〜1%未満)
- 発疹、蕁麻疹、そう痒感、紅斑
- 3. 過敏症
- (0.1%未満)
- 光線過敏性反応、顔面浮腫、リンパ節腫脹、多形紅斑、水疱性皮膚炎
- 4. 筋・骨格系
- (頻度不明)
- 関節痛
- 5. 筋・骨格系
- (0.1%未満)
- 筋肉痛
- 6. 肝臓
- (1%〜5%未満)
- γ-GTP上昇
- 7. 肝臓
- (0.1%〜1%未満)
- AST(GOT)、ALT(GPT)、LDH、ALPの上昇
- 8. 血液
- (1%〜5%未満)
- 白血球減少
- 9. 血液
- (0.1%〜1%未満)
- 貧血
- 10. 消化器
- (頻度不明)
- 膵炎
- 11. 消化器
- (1%〜5%未満)
- 胃部不快感
- 12. 消化器
- (0.1%〜1%未満)
- 腹痛、悪心、下痢、胃部膨満感、食欲不振、口渇
- 13. 消化器
- (0.1%未満)
- 嘔吐、舌炎
- 14. 精神神経系
- (頻度不明)
- 錯感覚、感覚鈍麻、不安、抑うつ
- 15. 精神神経系
- (0.1%〜1%未満)
- めまい、ふらつき、頭痛、眠気
- 16. 精神神経系
- (0.1%未満)
- 注意力低下、不眠、しびれ
- 17. 泌尿器
- (0.1%〜1%未満)
- BUN上昇
- 18. 泌尿器
- (0.1%未満)
- 頻尿
- 19. 感覚器
- (頻度不明)
- 嗅覚異常、聴覚障害、聴力低下、霧視、視力低下
- 20. 感覚器
- (0.1%〜1%未満)
- 味覚異常・味覚消失
- 21. 感覚器
- (0.1%未満)
- 耳鳴
- 22. その他
- (頻度不明)
- 乾癬、血管炎、インフルエンザ様疾患、体重減少
- 23. その他
- (0.1%〜1%未満)
- トリグリセライド上昇、総コレステロール上昇、疲労・けん怠感
- 24. その他
- (0.1%未満)
- 動悸、浮腫、月経異常、脱毛、発熱、CK(CPK)上昇
その他の副作用の注意
- 注)投与を中止し、適切な処置を行うこと。
注意事項
一般的名称: ;
貯法・使用期限等
- 貯法
- 室温保存
- 使用期限
-
包装に表示の使用期限内に使用すること
使用期限内であっても、開封後はなるべく速やかに使用すること
適用上の注意
- 眼科用として角膜、結膜には使用しないこと。誤って眼に入った場合は、刺激症状があらわれることがあるので、流水で十分に目をすすぐこと。
その他の注意
- 動物実験(モルモット)において、本剤に弱い光毒性が認められている。
一般的名称: ;
貯法・使用期限等
- 貯法
-
室温保存
火気を避けて保存すること
- 使用期限
-
包装に表示の使用期限内に使用すること
使用期限内であっても、開封後はなるべく速やかに使用すること
重要な基本的注意
- 本剤を乳児寄生菌性紅斑に使用する場合、アルコール性基剤(エタノール等)が局所刺激作用を有するため、注意して使用すること。
適用上の注意
- 1.
- 眼科用として角膜、結膜には使用しないこと。誤って眼に入った場合は、刺激症状があらわれることがあるので、流水で十分に目をすすぐこと。
- 2.
- 亀裂、びらん面には注意して使用すること。
一般的名称: ;
貯法・使用期限等
- 貯法
-
室温保存
火気を避けて保存すること
- 使用期限
-
包装に表示の使用期限内に使用すること
使用期限内であっても、開封後はなるべく速やかに使用すること
重要な基本的注意
- 本剤を乳児寄生菌性紅斑に使用する場合、アルコール性基剤(エタノール等)が局所刺激作用を有するため、注意して使用すること。
妊婦、産婦、授乳婦等への投与
- 妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。〔妊娠中の使用に関する安全性は確立していない。〕
小児等への投与
- 低出生体重児、新生児に対する安全性は確立していない(使用経験がない)。
適用上の注意
- 1.
- 点鼻用として鼻腔内に使用しないこと。
- 2.
- 顔面、頭部等、吸入する可能性のある患部には注意して使用すること。
- 3.
- 誤って眼に入った場合は、刺激症状があらわれることがあるので、流水で十分に目をすすぐこと。
一般的名称: ;
貯法・使用期限等
- 貯法
-
室温保存
開封後は光を避けて保存すること
- 使用期限
- 包装に表示の使用期限内に使用すること
慎重投与
(次の患者には慎重に投与すること)
- 1.
- 肝障害のある患者〔慢性もしくは活動性等の肝疾患を有する患者は肝障害が増悪するおそれがあるので、本剤の投与中は頻回に肝機能検査を行うなど、観察を十分に行うこと。〕(「副作用」の項参照)
- 2.
- 腎障害のある患者〔高い血中濃度が持続するおそれがある。〕
- 3.
- 高齢者(「高齢者への投与」の項参照)
重要な基本的注意
- 1.
- 重篤な肝障害(肝不全、肝炎、胆汁うっ滞、黄疸等)があらわれることがあり、死亡に至った例も報告されている。重篤な肝障害は主に投与開始後2ヵ月以内にあらわれるので、投与開始後2ヵ月間は月1回の肝機能検査を行うこと。また、その後も定期的に肝機能検査を行うなど観察を十分に行うこと。(「副作用」の項参照)
- 2.
- 汎血球減少、無顆粒球症及び血小板減少があらわれることがあるので、定期的に血液検査(血球数算定、白血球分画等)を行うなど観察を十分に行うこと。(「副作用」の項参照)
- 3.
- 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、急性全身性発疹性膿疱症、紅皮症(剥脱性皮膚炎)があらわれることがあるので、本剤の投与中は観察を十分に行うこと。(「副作用」の項参照)
- 4.
- 本剤の投与は、皮膚真菌症の治療に十分な経験を持つ医師のもとで、本剤の投与が適切と判断される患者についてのみ投与すること。
- 5.
- 本剤の投与にあたっては、添付文書を熟読し、本剤の副作用について患者に十分説明するとともに、異常が認められた場合には速やかに主治医に連絡するよう指示するなど注意を喚起すること。
- 6.
- 眠気、めまい・ふらつき等があらわれることがあるので、高所作業、自動車の運転等危険を伴う機械を操作する際には注意させること。
高齢者への投与
- 本剤は主として肝臓で代謝され、胆汁中及び尿中に排泄されるが、高齢者では一般に肝・腎機能が低下していることが多いため高い血中濃度が持続するおそれがあるので、副作用の発現に注意し、患者の状態を観察しながら慎重に投与すること。
妊婦、産婦、授乳婦等への投与
- 1.
- 妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。〔妊娠中の投与に関する安全性は確立していない。ウサギの器官形成期の大量投与(200mg/kg)により母獣の摂餌量の減少、体重増加の抑制が観察されている。〕
- 2.
- 授乳中の婦人には投与しないこと。やむを得ず投与する場合には、授乳を中止させること。〔動物実験(ラット)で乳汁中へ移行することが報告されている。〕
小児等への投与
- 低出生体重児、新生児、乳児、幼児又は小児に対する安全性は確立していない(使用経験がない)。
適用上の注意
- 薬剤交付時
- PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている)
その他の注意
- サルへの長期大量(150mg/kg以上)経口投与により網膜上に黄白色点が発現したとの報告があるので、本剤を6ヵ月以上の長期にわたり投与する場合には眼科学的検査を実施することが望ましい。
相互作用
相互作用
相互作用の概略
- 本剤は、主として肝代謝酵素チトクロームP450の分子種CYP2C9、CYP1A2、CYP3A4、CYP2C8、CYP2C19によって代謝され、また、CYP2D6を阻害する。
併用注意
(併用に注意すること)
-
1.
薬剤名等(1)シメチジン
(2)フルコナゾール - 臨床症状・措置方法
- 本剤の血中濃度が上昇するとの報告があるので、併用する場合には用量に注意すること。
- 機序・危険因子
- これらの薬剤によるチトクロームP450の抑制により本剤の代謝が遅延する。
-
2.
薬剤名等リファンピシン - 臨床症状・措置方法
- 本剤の血中濃度が低下するとの報告があるので、併用する場合には用量に注意すること。
- 機序・危険因子
- リファンピシンによる肝代謝酵素の誘導により、本剤の代謝が促進される。
-
3.
薬剤名等(1)三環系抗うつ剤(イミプラミン、ノルトリプチリン、アミトリプチリン)
(2)マプロチリン
(3)デキストロメトルファン - 臨床症状・措置方法
- これらの薬剤又はその活性代謝物の血中濃度が上昇することがあるので、併用する場合には用量に注意すること。
- 機序・危険因子
- 本剤のCYP2D6の阻害により、これらの薬剤又はその活性代謝物の代謝が遅延する。
-
4.
薬剤名等黄体・卵胞ホルモン混合製剤(経口避妊薬等) - 臨床症状・措置方法
- 月経異常があらわれたとの報告があるので注意すること。
- 機序・危険因子
- 機序不明。
-
5.
薬剤名等シクロスポリン - 臨床症状・措置方法
- シクロスポリンの血中濃度が低下したとの報告があるので、併用する場合にはシクロスポリンの血中濃度を参考にシクロスポリンの投与量を調節すること。特に、移植患者では拒絶反応の発現に注意すること。
- 機序・危険因子
- 機序不明。

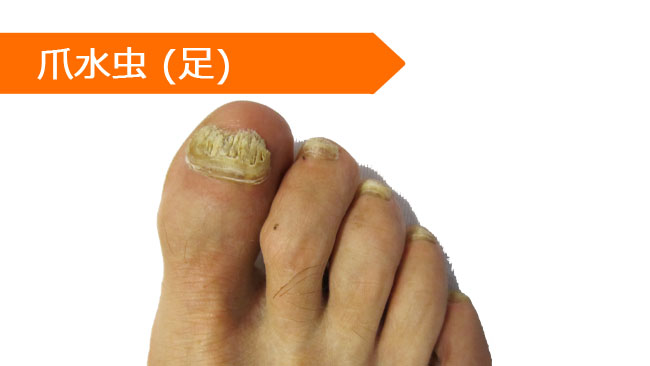





名前: 匿名 商品名: 症状: 爪水虫
医師に9ヶ月前にテルビナフィンを処方してもらいました。3ヶ月間服用し、その間2回肝臓のパネル検査を行いました。めまいと、最初の数日間の軽い吐き気、下痢がありました。新しい爪が生えてくるのに10ヶ月かかりましたが、もう一度つま先を見せられるようになりました!また、爪水虫だけでなく、足の皮膚の水虫も治りました。足が赤ちゃんのようにすべすべになり、乾燥やひび割れがありません。この薬はとてもお勧めです。待つのは時間の無駄です!きれいな足を取り戻すことができました!
名前: 匿名 商品名: 症状: 爪水虫
足の指10本全て、水虫で茶色く変色しており、裸足になるときは本当に恥ずかしかったです。何とかしようと決め、テルビナフィンのことを知り、この薬について色々と調べましたが、副作用のリスクが心配だったので、すべての指にレーザー治療を行いました。5ヶ月も経っても状態は変わらず、がっかりしてまた医者に行くと、テルビナフィンがこの水虫には一番良く効くと言われ、かなり悩んだ結果、テルビナフィンを服用することに決めました。病院で肝臓検査をしてもらいましたが、全て大丈夫でした。3ヶ月この薬を飲み、本当に決めて良かったです!茶色の爪はほとんどなくなり、新しい爪が伸びてきています。そして、副作用もありませんでした。
足の指10本全て、水虫で茶色く変色しており、裸足になるときは本当に恥ずかしかったです。何とかしようと決め、テルビナフィンのことを知り、この薬について色々と調べましたが、副作用のリスクが心配だったので、すべての指にレーザー治療を行いました。5ヶ月も経っても状態は変わらず、がっかりしてまた医者に行くと、テルビナフィンがこの水虫には一番良く効くと言われ、かなり悩んだ結果、テルビナフィンを服用することに決めました。病院で肝臓検査をしてもらいましたが、全て大丈夫でした。3ヶ月この薬を飲み、本当に決めて良か
スポンサーリンク
名前: 匿名 商品名: 症状: 爪水虫
12歳のころから足の指10本全てにある、忌まわしき水虫。もう52歳です。人生が変わりました。子供の頃から今まで、自分のつま先を隠しながら、なるべく笑われたり恥ずかしい思いをしないように暮らしてきました。今、4ヶ月間この薬を服用しています。驚きです。親指の爪はもう半分きれいになり、他の8つの爪はもう9割方きれいになりました。一時的に味覚の副作用がありましたが、肝機能は正常です。試してみることをオススメします。
名前: 匿名 商品名: 症状: 爪水虫
私は少なくとも18年間、アスリートの足を扱ってきました。私はかゆみ、鱗屑、厚い肌、臭い、そして厚い、茶色の、込められた爪のはいを扱った。私はそれを取り除くために太陽の下ですべてを試みました。私はアップルサイダービネガーに足を浸すか、またはVicks蒸気を使って爪をこするような家庭の救済策を試みました。私がこれらの「治療法」のどれかで何かを成し遂げたならば、菌類を守ることはほぼ終わりです。いいえ、悪くはありません。だから私は最終的にそれについて何かをし、ラミスの錠剤を試してみることにしました。 2012年10月に開始され、2012年12月に終了しました。その今6月/ 2013と私の爪は10倍良く見える。濃い、茶色がかった色は消えてしまった。内釘なし。私は今サンダルを履くことができます!
私は少なくとも18年間、アスリートの足を扱ってきました。私はかゆみ、鱗屑、厚い肌、臭い、そして厚い、茶色の、込められた爪のはいを扱った。私はそれを取り除くために太陽の下ですべてを試みました。私はアップルサイダービネガーに足を浸すか、またはVicks蒸気を使って爪をこするような家庭の救済策を試みました。私がこれらの「治療法」のどれかで何かを成し遂げたならば、菌類を守ることはほぼ終わりです。いいえ、悪くはありません。だから私は最終的にそれについて何かをし、ラミスの錠剤を試してみることにしました。 2
名前: 匿名 商品名: 症状: 爪水虫
子供のころから足水虫と、爪水虫で苦しんできました。40歳です。テルビナフィンの錠剤で90日間の治療を開始しました。人生が変わったと思います。副作用はありませんでした。長い間人生で苦しんできた、この水虫がなくなってきています。サンダルを履いたり、裸足で歩いたりできず、常に恥ずかしい思いをしていました。今、私の足は正常になりました。1ヶ月以内に効果が出始め、かゆみや痛みがなくなった。 2ヶ月目には、爪が黒から透明に変わってきました。8ヶ月前に薬を服用し始め、3ヶ月間服用しました。今では、爪も足も完全にキレイになりました。
子供のころから足水虫と、爪水虫で苦しんできました。40歳です。テルビナフィンの錠剤で90日間の治療を開始しました。人生が変わったと思います。副作用はありませんでした。長い間人生で苦しんできた、この水虫がなくなってきています。サンダルを履いたり、裸足で歩いたりできず、常に恥ずかしい思いをしていました。今、私の足は正常になりました。1ヶ月以内に効果が出始め、かゆみや痛みがなくなった。 2ヶ月目には、爪が黒から透明に変わってきました。8ヶ月前に薬を服用し始め、3ヶ月間服用しました。今では、爪も足も完全
名前: 匿名 商品名: 症状: 爪水虫
この薬を3週間服用して、味覚が無くなりました。2週間で、6キロ痩せました。この副作用はまれだと言う人がいますが、他にも同じような経験をした人がいます。時間とお金も無駄になりました。うつになり、病気にもかかり、つねに衰弱しているのに、イライラしていました。そして、まだ足の爪は変化なしです。
名前: 匿名 商品名: 症状: 爪水虫
常にサンダルやつま先が見える靴を履くことが恥ずかしく、色々な楽しみを逃して来ました。女の子なので、みんながかわいい靴を履いているのを見て、私も履いてみたいと思いました。約8ヶ月かかりましたが、水虫は完治しました!本当に奇跡の薬でした!足の水虫で悩んでいる人に、お勧めします。今では履きたい靴を履いてもなんの問題もありません。唯一後悔しているのは、もっと早くやればよかったことです。
スポンサーリンク
名前: 匿名 商品名: 症状: 爪水虫
3ヶ月の治療を完了してから2週間経ちますが、特に問題や副作用はありませんでした。インターネットにあふれるネガティブレビューを読んでいたので、治療前はテルビナフィンを服用するのはとても心配でした。爪はどんどんきれいになっており、水虫の爪は成長しておらず、新しい健康な爪が生えてきています。本当に素晴らしい薬です。テルビナフィンを始めてから6キロほど痩せたし、アレルギーも出なくなりました。長い間花粉症にも悩まされていますが、今年の春は、鼻水や眼の痒みが出ませんでした。本当にうれしいです!
3ヶ月の治療を完了してから2週間経ちますが、特に問題や副作用はありませんでした。インターネットにあふれるネガティブレビューを読んでいたので、治療前はテルビナフィンを服用するのはとても心配でした。爪はどんどんきれいになっており、水虫の爪は成長しておらず、新しい健康な爪が生えてきています。本当に素晴らしい薬です。テルビナフィンを始めてから6キロほど痩せたし、アレルギーも出なくなりました。長い間花粉症にも悩まされていますが、今年の春は、鼻水や眼の痒みが出ませんでした。本当にうれしいです!
名前: 匿名 商品名: 症状: 爪水虫
32年前に仕事の訓練中に水虫にかかりました。市販のクリームを色々と試しましたが、一時的な効果しかありませんでした。17年前に皮膚科に行き、テルビナフィンの錠剤を1日1回12日間処方してもらいました。かゆみと痛みは3日後に消えましたが、そのまま処方された薬を全て飲みきりました。その後今まで水虫は出ていません。素晴らしい薬です。
名前: 匿名 商品名: 症状: 爪水虫
あと8日分残っていますが、副作用は特にありませんでした。親指の爪が服用後10日後にキレイになりはじめました。もう根本から5ミリほどきれいな爪が伸びてきています。医師には、治療開始からきれいな爪が完全に完全に成長するまで9ヶ月ほどかかるかもしれないと言われています。 他の水虫の爪2つも明らかにキレイになってきていますが、小指の爪だけはまだ変化がありません。
名前: 匿名 商品名: 症状: 爪水虫
何年も足の爪の水虫に悩まされてきました。他の薬を使ってみましたが、効果はありませんでしたが、テルビナフィンは2ヶ月で完全にキレイになりました。医者には、結果が出るまでに6ヶ月から1年かかることがあると言われましたが、ありがたいことに、それほど待つ必要はありませんでした。
名前: 匿名 商品名: 症状: 爪水虫
こちらのレビューを読んだ後、実体験に基づいてレビューを書くつもりでこの薬を始めました。約6ヶ月間テルビナフィン錠を服用しています。副作用は無く、血液検査を一回受けましたが、臓器には異常ありませんでした。こちらでつま先が1ヶ月以内にキレイになり始めたというレビューを読みましたが、私はそうではありませんでした。通常は、爪水虫の真菌が死に、新しい爪が成長し始めるまで、改善は見られないようです。このような状態になるまでに1年以上かかることもあるようです。私の場合は、約10-11ヶ月だったと思います。服用を終えてから4か月かかりました。服用を終えた時点では、私の爪は薬を飲み始めたときとほとんど変わりませんでした。そして、魔法のように新しいきれいな爪が生えてきました。この段階で、すべて靴下と靴を捨てて、新しいものを買いました。足の爪はゆっくり伸びますよ!
こちらのレビューを読んだ後、実体験に基づいてレビューを書くつもりでこの薬を始めました。約6ヶ月間テルビナフィン錠を服用しています。副作用は無く、血液検査を一回受けましたが、臓器には異常ありませんでした。こちらでつま先が1ヶ月以内にキレイになり始めたというレビューを読みましたが、私はそうではありませんでした。通常は、爪水虫の真菌が死に、新しい爪が成長し始めるまで、改善は見られないようです。このような状態になるまでに1年以上かかることもあるようです。私の場合は、約10-11ヶ月だったと思います。服用
スポンサーリンク
名前: 匿名 商品名: 症状: 爪水虫
これまでに非常に高価な薬も試してきましたが、その薬よりはるかに効果的です。この薬は安く手に入るので素晴らしいです。3ヶ月経ちますが、まだ完全に水虫がなくなったわけではありませんが、まだキレイになってきており、足の指はとてもキレイになっています。真菌性の爪水虫でお困りの方にはお勧めです。
名前: 匿名 商品名: 症状: 爪水虫
31歳の女性です。10年以上足に水虫がありました。片方の足の親指と小指でした。2ヶ月前に親指の爪がとても痛く(虫歯のような痛み)なったので、医者に行きました。テルビナフィンを処方されました。副作用は食欲不振でしたが、残念ながら1週間経つと食欲は復活しました。 その他に、2回は胃が軽い痙攣を起こし、最初の1週間ぐらいは普段より少し疲労感がありましたが、その後は副作用はありませんでした。今38日目です。きれいな爪が伸びてきているのでとてもうれしいです!爪が完全に伸びきるまで、あと6ヶ月位かかるかもしれませんので、油断はできませんが、確かに効果があります!
31歳の女性です。10年以上足に水虫がありました。片方の足の親指と小指でした。2ヶ月前に親指の爪がとても痛く(虫歯のような痛み)なったので、医者に行きました。テルビナフィンを処方されました。副作用は食欲不振でしたが、残念ながら1週間経つと食欲は復活しました。 その他に、2回は胃が軽い痙攣を起こし、最初の1週間ぐらいは普段より少し疲労感がありましたが、その後は副作用はありませんでした。今38日目です。きれいな爪が伸びてきているのでとてもうれしいです!爪が完全に伸びきるまで、あと6ヶ月位かかるかもし
名前: 匿名 商品名: 症状: 爪水虫
4週間テルビナフィンを服用しました。看護師をしていますが、この薬が味覚に影響を与える可能性があることを知りませんでした。過去最悪の副作用でした。味覚の変化は一晩で起こりました。突然すべてがエンジンオイルのような味になり、7日間薬を飲んでいませんが、まだまともに食事をすることができません。なんとか味覚が戻ってくるように祈る毎日です。
名前: 匿名 商品名: 症状: 爪水虫
ほぼ3ヶ月使用しました。筋肉の痛みが出たので、医者が薬を中断しました。それ以外特に問題はなく、つま先は3ヶ月後にはとてもキレイになりました。35年間自分なりに色々と試して来ましたが、効果はありませんでした。妻は、この夏にはサンダルを着用してほしいと言っています。17歳のころ以来です。親指は約75%、他の指は約90%きれいになっています。裸足でビーチを歩けるようになるのが楽しみです。
名前: 匿名 商品名: 症状: 爪水虫
5ヶ月間使用していますが、医師にあと1ヶ月頑張りましょうと言われました。 二箇所の爪に水虫があり、親指は8割方感染していたのが、あと約15%を残すのみになっています。最初の3〜4ヶ月は爪の改善が非常に遅かったのですが、今月に入ってからは毎日改善しています。ありがたいことに、最初の数日間の胃の痛み以外の副作用はありませんでした。毎月の血液検査で、肝臓の酵素も正常なのを確認しています。
スポンサーリンク
名前: 匿名 商品名: 症状: 爪水虫
テルビナフィンのジェネリック医薬品を3ヶ月間使用しており、あと約1週間分残っています。足の爪(そのうち4つはひどい水虫で、残りはすこし黄色っぽくなっています)は明らかに改善してきていると思います。私は副作用が心配で何年もこの薬を飲むのを拒否してきましたが、この薬で副作用はなく、恥ずかしい思いをしてきたのがバカみたいです。迷っている人は試してみることをお勧めします。まだ3ヶ月間過ぎていませんが、試してみてよかったです!
名前: 匿名 商品名: 症状: 爪水虫
23年前に大学のシャワー室で水虫にかかり、すぐに爪まで広がってしまいました。水虫を治したり、隠したり、色々と試してきました。左足だけしかかかっていませんでしたが、つま先はひどい状態でした。反対の足と比べて3倍の厚さで、かなり汚かったです。見られる可能性があるときは、テープを巻いて怪我をしたふりをしていました。テルビナフィンを30日以上服用しましたが、爪はきれいになってきており、親指も見違えるようです。この水虫を隠すのに20年以上悩まされてきましたが、もう見られても大丈夫です。解放されました。本当に素晴らしい薬ですが、変な夢を見たり、不眠症になったりという副作用はありました。
23年前に大学のシャワー室で水虫にかかり、すぐに爪まで広がってしまいました。水虫を治したり、隠したり、色々と試してきました。左足だけしかかかっていませんでしたが、つま先はひどい状態でした。反対の足と比べて3倍の厚さで、かなり汚かったです。見られる可能性があるときは、テープを巻いて怪我をしたふりをしていました。テルビナフィンを30日以上服用しましたが、爪はきれいになってきており、親指も見違えるようです。この水虫を隠すのに20年以上悩まされてきましたが、もう見られても大丈夫です。解放されました。
名前: 匿名 商品名: 症状: 爪水虫
テルビナフィンを1月服用したところです。いくつか副作用はありましたが、まだ服用を続けるつもりです。好きな靴をどれでも履けるようになるのが待ちきれません。もうこの水虫との付き合いも長くなりますが、ここで決着をつけたいです。すでにかなり効果が出てきています。
名前: 匿名 商品名: 症状: 爪水虫
31歳女性です。 テルビナフィンを2ヶ月半服用しており、副作用はありません。もう爪は見違えるようになっています!
名前: 匿名 商品名: 症状: 爪水虫
7週間テルビナフィンを服用しました。味覚がなくなり、少し疲労感もあります。味覚がなくなったのは心配です。味覚がすぐに戻って来る人もいれば、何ヶ月経っても戻らない人もいるみたいです。水でさえまずく感じます。爪はきれいになってきたので、完治するまで続けるつもりですが、味覚が戻ってくるように祈る思いです。甘いものを食べたくならないのは良いんですが、美味しいお酒の味が恋しいです。うまくいきますように!
スポンサーリンク
名前: 匿名 商品名: 症状: 爪水虫
足の指10本全てひどい水虫に感染した状態でほぼ6年間苦しみました。見た目は最悪でした!!!常に靴下をつけて靴を履かないといけませんでした。この薬で3ヶ月服用して治療し、明らかに改善しました!が、治療が終わってから3ヶ月後でも、水虫菌はまだ頑固に私の爪に残っていたので、お医者さんにもう一回治療をお願いしました。この治療を終え、今ではきれいな爪10個が私の足に並んでいます!何年かぶりに、ペディキュアをして、サンダルを買いあさりました!!私の場合は副作用も特にありませんでした。心配していましたが、どんな薬にもリスクが有ります。思い切ってやってみて良かったです!
足の指10本全てひどい水虫に感染した状態でほぼ6年間苦しみました。見た目は最悪でした!!!常に靴下をつけて靴を履かないといけませんでした。この薬で3ヶ月服用して治療し、明らかに改善しました!が、治療が終わってから3ヶ月後でも、水虫菌はまだ頑固に私の爪に残っていたので、お医者さんにもう一回治療をお願いしました。この治療を終え、今ではきれいな爪10個が私の足に並んでいます!何年かぶりに、ペディキュアをして、サンダルを買いあさりました!!私の場合は副作用も特にありませんでした。心配していましたが、どん
名前: 匿名 商品名: 症状: 爪水虫
この薬で2度治療しました。1回目のときは全然効果が無いように感じました。 2回目に時には、爪を削ってから3ヶ月間服用し、見事に治りました。この薬はお勧めです。肝臓や腎臓に負担をかけないように、アルコールは控えましょう。素晴らしい薬です!
名前: 匿名 商品名: 症状: 爪水虫
足の指の爪の伸びる速さは人によって違います。ゆっくり伸びる人の場合は、治るまでに1年間かかることがあります。3週間ジェネリックのテルビナフィンを服用しており、すでに5個すべての足の爪の根本からきれいな爪が生えてきています。まだ治療は続けています。キレイに見えるようになったからといって、水虫の真菌が完全になくなったわけではありません。私の場合はすぐに治り始めたので、過度に期待して治療を始めてもすぐに改善が見られずがっかりしてしまうかもしれませんが、それぞれ症状や条件が違いますので、治療をしっかり進めれば確実に効果があると思います。
足の指の爪の伸びる速さは人によって違います。ゆっくり伸びる人の場合は、治るまでに1年間かかることがあります。3週間ジェネリックのテルビナフィンを服用しており、すでに5個すべての足の爪の根本からきれいな爪が生えてきています。まだ治療は続けています。キレイに見えるようになったからといって、水虫の真菌が完全になくなったわけではありません。私の場合はすぐに治り始めたので、過度に期待して治療を始めてもすぐに改善が見られずがっかりしてしまうかもしれませんが、それぞれ症状や条件が違いますので、治療をしっかり進